

發布時間:2024-01-04 21:02:00
大腦運作依賴復雜而高效的血管網絡為其提供營養物質并帶走代謝廢物。為維持神經組織的穩態和正常神經活動,腦血管在發育過程中形成了血腦屏障,以嚴格控制血液與腦實質之間的物質交換。血腦屏障的異常與包括阿茲海默癥在內的多種腦疾病緊密相關。周細胞作為毛細血管中貼附內皮細胞管腔外側的壁細胞,對維持血腦屏障的完整性起到關鍵作用。因此,解析大腦周細胞的發育過程對探索血腦屏障的形成和維持的機制至關重要。先前的研究表明,血流作為血管最重要的功能表現形式,參與調節了大腦血管內皮細胞的發育。然而,血流是否影響大腦周細胞的發育目前仍不清楚。
研究人員利用斑馬魚作為模式脊椎動物,通過CRISPR/Cas9基因敲入技術構建了特異性標記周細胞的在體研究模型。通過在體長時程連續成像,發現大腦周細胞最早來源于腦周血管上的前體細胞,遷移入腦后在腦內進行分裂,這是腦內周細胞數目增長的主要方式。通過藥理學手段改變血流速度,發現血流上調大腦血管上周細胞的覆蓋密度,這種調節主要是通過促進大腦周細胞的分裂實現的。進一步地,研究人員發現,血管內皮細胞上表達的機械敏感性陽離子通道Piezo1感應血流變化,介導血流對周細胞分裂的調節。
血流的作用是如何從血管內皮細胞傳遞到周細胞的呢?研究人員發現,Piezo1的激活顯著提高了內皮細胞中Notch信號的活性。特異性升高或抑制血管內皮細胞內在的Notch信號活性,導致大腦周細胞的分裂速率出現相應的上調或下調。在血管內皮細胞Notch信號被抑制的情況下增加血流速度和Piezo1活性,均無法引起大腦血管上周細胞密度發生明顯的變化,表明血管內皮細胞內在的Notch信號作為Piezo1的下游介導了血流對大腦周細胞發育的調節。此外,通過特異性增強或抑制血管內皮細胞中Notch信號的向外傳遞,研究人員進一步提供了血管內皮細胞中Notch信號直接激活周細胞中的Notch信號進而促進周細胞分裂的證據。
該研究揭示了血流調控腦血管發育的新機制,為進一步研究大腦周細胞的發育提供了新視角。同時,對于正在努力尋找治療神經系統疾病方法的研究人員來說,這一發現可能提供新的治療策略。例如,通過上調血管內皮細胞中Piezo1活性或者Notch信號強度,有助于增加周細胞的增殖,從而改善腦血管功能,有利于阿茲海默癥、血管性癡呆、腦卒中等疾病患者腦功能的恢復。
杜久林研究員與李佳副研究員為本論文的通訊作者,杜久林組博士后訾化星為本論文的第一作者,助理研究員彭小蘭參與了該課題中的斑馬魚在體動態成像實驗,研究生解天意、劉亭亭博士、李紅羽博士和卜紀雯對課題中涉及的重要斑馬魚品系的制作做出了重要貢獻;此外,溫州醫科大學附屬浙江省臺州醫院曹建斌參與了該課題的藥理學實驗;中國科學院腦智卓越中心光學平臺提供了重要技術支持。該研究獲得了科技部國家重點研發計劃、國家自然科學基金、上海市自然科學基金、SA-SIBS優秀人才獎勵基金和中國科學院青促會的資助。
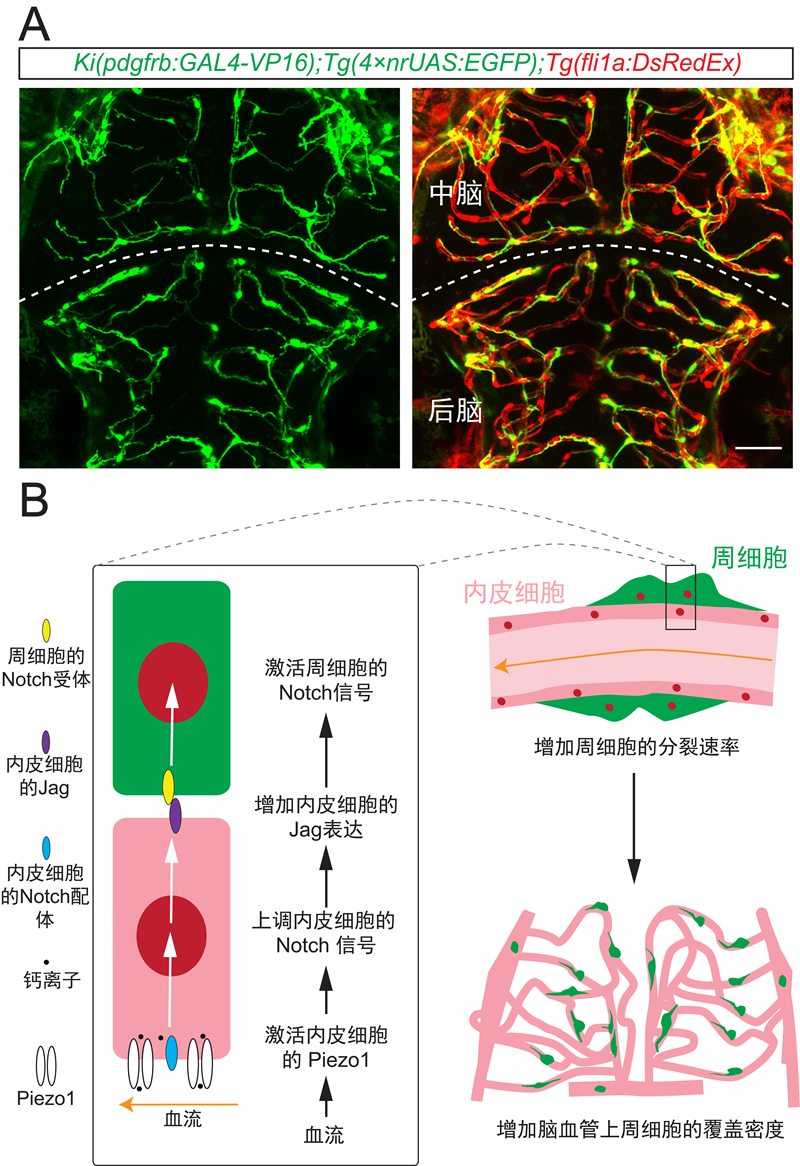
A. 斑馬魚胚胎大腦血管(紅色)和周細胞(綠色)的在體成像。B. 血流調節大腦周細胞發育的機制模式圖。血流激活血管內皮細胞的Piezo1,引起內皮細胞Notch信號的上調,促使血管內皮細胞表達更多的Notch配體Jag,進而激活周細胞中的Notch信號,最終促進大腦周細胞的分裂,增加其對腦血管的覆蓋。
 附件下載:
附件下載: