



發(fā)布時間:2021-01-05 00:00:00
2021年1月5日,《Nature Cell Biology》期刊在線發(fā)表了題為《通過內(nèi)源性啟動子驅(qū)動的sgRNA監(jiān)測低豐度轉(zhuǎn)錄本和lncRNAs的表達》的研究論文,該研究由中國科學院腦科學與智能技術(shù)卓越創(chuàng)新中心(神經(jīng)科學研究所)、上海腦科學與類腦研究中心、神經(jīng)科學國家重點實驗室楊輝研究組和周海波研究組合作完成。該研究通過內(nèi)源基因的啟動子驅(qū)動sgRNA(single-guide RNAs)表達,結(jié)合SPH-OminiCMV(CRISPR-activator Suntag-P65-HSF1 and OminiCMV-mCherry)熒光報告系統(tǒng),成功實現(xiàn)低豐度基因和lncRNAs(Long non-coding RNAs)基因表達的動態(tài)示蹤。該研究建立了一種通用的內(nèi)源基因轉(zhuǎn)錄門控系統(tǒng),為活細胞中實時標記低表達基因和lncRNAs,研究其生物學功能提供了有效工具。
在活細胞中實時監(jiān)測內(nèi)源基因活性對于研究基因的生物學功能并調(diào)控其表達水平至關(guān)重要。近年來越來越多證據(jù)表明,lncRNAs通過調(diào)控某些重要編碼基因的表達,不僅參與了腦發(fā)育、神經(jīng)元分化、突觸可塑性的發(fā)生發(fā)展,而且參與神經(jīng)系統(tǒng)損傷之后的修復過程。深入研究lncRNAs,將為治療神經(jīng)系統(tǒng)疾病提供新思路。但是受現(xiàn)有標記技術(shù)的限制,對其功能注釋極具挑戰(zhàn)性。
監(jiān)測內(nèi)源基因活性的常規(guī)方法是將熒光蛋白精確插入蛋白編碼框中,但是,這種方法并不適用于非編碼基因和低豐度轉(zhuǎn)錄的基因。sgRNA,類似于一個GPS可以將Cas核酸酶直接導向目標核酸位點,具有高特異性、高效率和多功能性。盡管各種誘導性sgRNA已經(jīng)被開發(fā)用來接收活細胞中的內(nèi)源信號,但這些方法只能用于某些功能明確的小RNA的反應。目前在活細胞里面標記內(nèi)源基因表達的方法,都具有一定的局限性,而且,對于低表達的基因以及lncRNA,目前缺乏很好的活細胞內(nèi)的標記技術(shù)。 建立適用范圍更廣,能增強內(nèi)源信號,并且信噪比更低的新型活細胞標記技術(shù),是該研究領(lǐng)域急需解決的問題。
楊輝研究組和周海波研究組合作開發(fā)了一種廣譜的內(nèi)源性轉(zhuǎn)錄門控開關(guān)Ents(Endogenous Transcription-Gated Switch),利用內(nèi)源性啟動子表達sgRNA前體,之后sgRNA前體上的tRNA序列可以被內(nèi)源的自剪切機制識別并且切割,進而釋放出能夠執(zhí)行功能的sgRNA,當Ents與高度敏感的CRISPR激活相關(guān)的報告系統(tǒng)SPH-OminiCMV結(jié)合,可以監(jiān)測到內(nèi)源基因的表達(圖A)。值得注意的是,SPH-OminiCMV-Ents能夠放大內(nèi)源信號,從而實現(xiàn)低豐度轉(zhuǎn)錄本表達的可視化。
為進一步研究SPH-OminiCMV-Ents用于監(jiān)測內(nèi)源基因的能力,團隊選取了表達量從高到低的八個基因,發(fā)現(xiàn)SPH-OminiCMV-Ents誘導的mCherry表達水平普遍高于常用的P2A-mCherry標記策略,尤其是P2A-mCherry策略標記后在熒光顯微鏡下幾乎無信號的低豐度表達基因Sox2、Tet1、Sall4、Tbx3等(圖B)。
為探討增加sgRNA拷貝數(shù)是否會進一步增強熒光蛋白的產(chǎn)生,團隊構(gòu)建了一個sgRNA前體,包含六到八個串聯(lián)的sgRNA拷貝,每個sgRNA的兩側(cè)分布著tRNA序列(圖C)。研究表明,插入sgRNA陣列可以對低豐度基因?qū)崿F(xiàn)更好的監(jiān)測,比如lncRNA Tug1,當僅用一個拷貝的sgRNA的時候不能監(jiān)測到其表達,但使用sgRNA陣列則可以(圖D,E)。
為進一步探討此方法的特性,團隊成員建立了一個可控的Tet-on系統(tǒng),該系統(tǒng)可以通過調(diào)節(jié)Dox的濃度,實現(xiàn)EGFP基因不同程度的表達量,進而用來研究報告系統(tǒng)的熒光信號強度是否可以很好地反映目標基因的表達水平。研究發(fā)現(xiàn),報告系統(tǒng)的mCherry表達量和EGFP基因的表達量有很強的相關(guān)性,并且進一步探索了此報告系統(tǒng)和目標基因表達在轉(zhuǎn)錄本水平和蛋白翻譯水平存在的時間差(圖F)。
為探討此系統(tǒng)是否能夠隨著基因表達量的增高,其報告系統(tǒng)也能監(jiān)測出信號增強的變化。團隊選取了表達量在小鼠胚胎干細胞中表達量低,但體外分化成神經(jīng)元后表達量會增高的Tubb3基因。實驗結(jié)果顯示,分化后Tubb3的基因表達量不管是mRNA還是蛋白水平的表達量均增高,報告系統(tǒng)中的紅色熒光信號也隨之增高,能夠反映基因表達的動態(tài)變化。
該研究創(chuàng)新開發(fā)了由內(nèi)源性啟動子驅(qū)動的高度可編程的sgRNA門控開關(guān)Ents,此系統(tǒng)理論上可以處理任何轉(zhuǎn)錄本的信息。研究人員將Ents與SPH-OminiCMV結(jié)合使用,在小鼠胚胎干細胞水平上實現(xiàn)了對低豐度基因和lncRNA的可視化監(jiān)測及其動態(tài)變化的監(jiān)測。該研究為在活細胞中研究基因元件的功能開辟了新途徑,在動物個體水平可用于描繪基因表達的時空圖譜和標記、鑒定特定的細胞類群,同時可用于研究天使綜合癥等疾病中l(wèi)ncRNA的表達模式,構(gòu)建lncRNA體內(nèi)表達完整圖譜。
該研究由博士研究生高妮、博士后胡靜、賀冰冰、碩士研究生基正邦,以及博士后胡新德,在楊輝研究員和周海波研究員的共同指導下完成,研究組的其他成員積極參與。該研究得到了腦智卓越中心基因編輯平臺、分子流式平臺、光學成像平臺的大力支持,獲得中國科學院、國家自然科學基金委、上海市科委的資助。
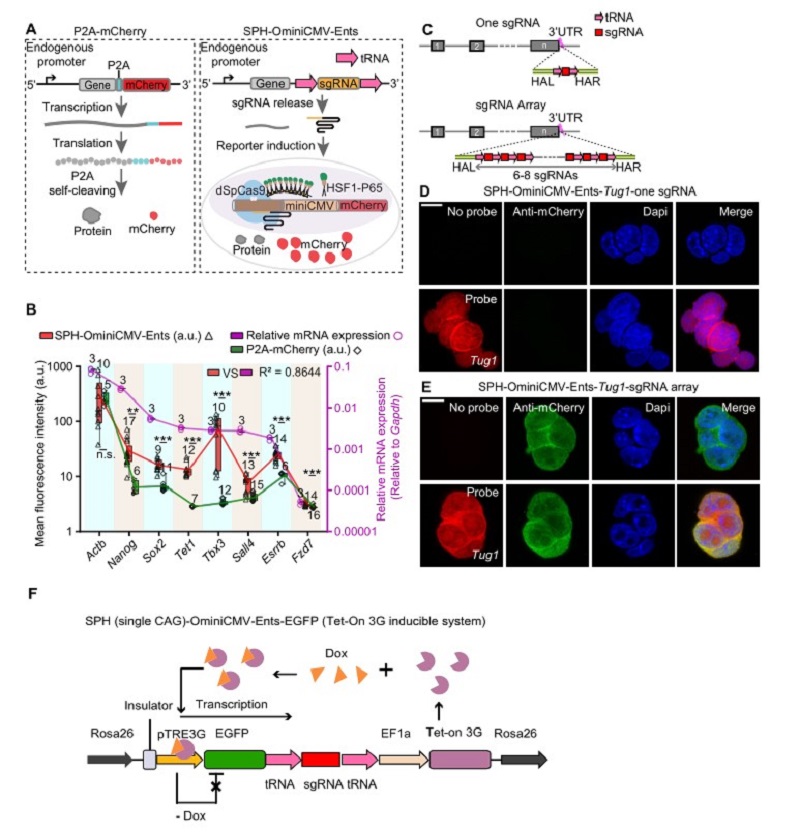
圖注1:(A)示意圖顯示P2A-mcherry和SPH-OminiCMV-Ents兩種標記基因的策略。(B)在mESC細胞中用SPH-OminiCMV-Ents策略(紅色三角形)和P2A- mCherry策略(綠色菱形)標記不同的基因,統(tǒng)計其mCherry熒光信號強度以及用qPCR分析這些基因的表達水平(紫色圓圈,紫色y軸)。(C)示意圖顯示插入一個sgRNA或一個sgRNA陣列的標記策略。(D,E)Fish圖像顯示對lncRNA Tug1在3'UTR中插入一個sgRNA或一個sgRNA陣列后,細胞系中mCherry報告熒光信號的表達情況。(F)可控的Tet-on系統(tǒng)示意圖,Dox誘導EGFP-sgRNA前體轉(zhuǎn)錄,成熟的sgRNA釋放出來激活mcherry報告系統(tǒng)。
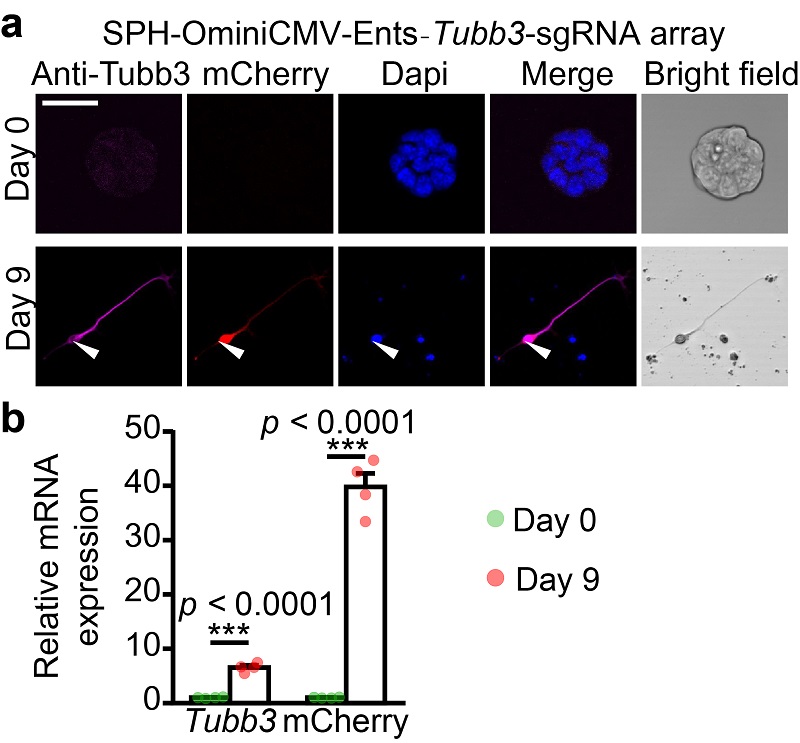
圖注2:(A)在小鼠的胚胎干細胞上標記Tubb3基因,體外分化成神經(jīng)元后,Tubb3基因表達量升高,標記到的紅色報告熒光也從極低到高。(B)分化前和分化后Tubb3基因和報告熒光信號在mRNA水平升高的量化統(tǒng)計。
研究組之前的研究成果——SPH激活系統(tǒng):
 附件下載:
附件下載: