發(fā)布時(shí)間:2025-11-14
2025年11月4日,中國(guó)科學(xué)院腦科學(xué)與智能技術(shù)卓越創(chuàng)新中心師詠勇研究團(tuán)隊(duì)聯(lián)合上海交通大學(xué)、山東大學(xué)、青島大學(xué)、安徽醫(yī)科大學(xué)等高校的團(tuán)隊(duì)在Nature Genetics期刊上發(fā)表題為“Multi-ancestry genome-wide association analyses of polycystic ovary syndrome”的研究論文。該研究繪制了全球多囊卵巢綜合征(PCOS)精細(xì)遺傳圖譜,鑒定出94個(gè)獨(dú)立遺傳位點(diǎn),包含73個(gè)首次報(bào)道位點(diǎn);揭示了歐亞不同人群PCOS代謝驅(qū)動(dòng)與生殖驅(qū)動(dòng)的異質(zhì)性;構(gòu)建出多基因風(fēng)險(xiǎn)評(píng)分模型,全面分析了PCOS的致病通路與調(diào)控機(jī)制,為深入理解其復(fù)雜遺傳結(jié)構(gòu)及開(kāi)發(fā)精準(zhǔn)治療策略提供了重要理論基礎(chǔ)與轉(zhuǎn)化視角。
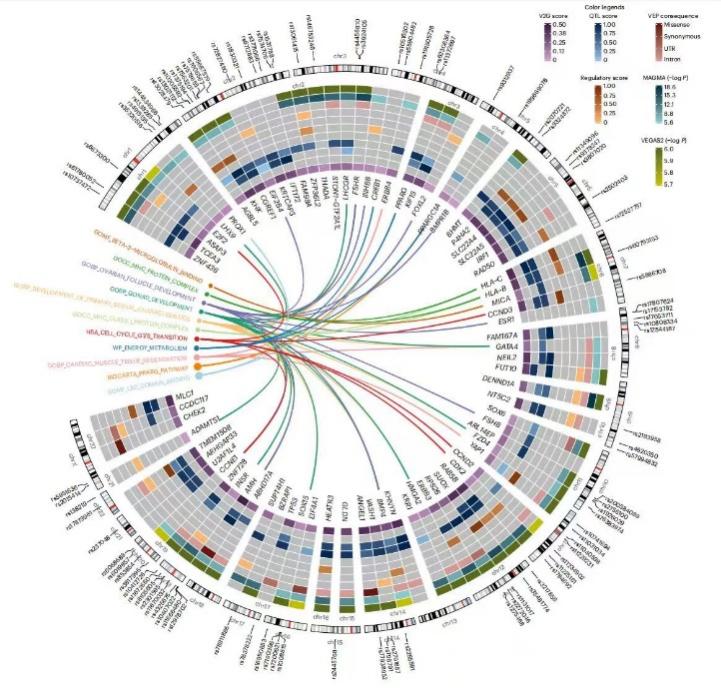
PCOS是育齡女性最常見(jiàn)的生殖內(nèi)分泌代謝性疾病,嚴(yán)重影響女性生殖健康,常合并抑郁、焦慮、肥胖、胰島素抵抗和2型糖尿病等臨床表型。PCOS具有明顯家族聚集性和高度遺傳性,系統(tǒng)解析其遺傳結(jié)構(gòu)一直是該領(lǐng)域的研究重點(diǎn)與難點(diǎn)。
為破解 PCOS 遺傳密碼,研究團(tuán)隊(duì)在先前基礎(chǔ)上,依托PCOS專病隊(duì)列,納入12419名中國(guó)PCOS患者和34235名對(duì)照開(kāi)展全基因組關(guān)聯(lián)分析,繼而整合歐洲人群數(shù)據(jù)進(jìn)行跨祖先薈萃分析,最終鎖定94個(gè)位點(diǎn)。功能注釋發(fā)現(xiàn),位于AMH基因上的錯(cuò)義突變rs10407022在東亞人群中效應(yīng)更強(qiáng),可能與PCOS患者卵泡數(shù)量增多和雄激素水平升高相關(guān)。基因富集分析提示,PCOS相關(guān)基因顯著富集于PPARG信號(hào)通路等過(guò)程,且單細(xì)胞RNA測(cè)序數(shù)據(jù)表明,這些基因在卵巢顆粒細(xì)胞中活躍表達(dá)。
通過(guò)跨人群精細(xì)定位技術(shù)(SuSiEx),研究團(tuán)隊(duì)精準(zhǔn)篩選出多個(gè)高可信度的潛在因果變異。雙向孟德?tīng)栯S機(jī)化分析則系統(tǒng)揭示了PCOS與心臟代謝指數(shù)及生殖性狀的因果關(guān)系。值得關(guān)注的是,該研究還系統(tǒng)對(duì)比了漢族與歐洲人群的遺傳特征,發(fā)現(xiàn)兩者存在顯著的遺傳重疊,但也存在明顯差異:漢族人群PCOS遺傳度更高,且代謝相關(guān)基因承受的選擇壓力更為顯著;而歐洲人群中生殖相關(guān)基因的選擇信號(hào)更強(qiáng)。這提示不同人群的PCOS發(fā)病可能分別存在“代謝驅(qū)動(dòng)”或“生殖驅(qū)動(dòng)”的特點(diǎn)。
團(tuán)隊(duì)進(jìn)一步構(gòu)建適用于多種族的多基因風(fēng)險(xiǎn)評(píng)分(PRS)模型,風(fēng)險(xiǎn)比高達(dá)13.63倍,展現(xiàn)出優(yōu)異的疾病分層能力。在藥物研發(fā)探索中,研究不僅從遺傳層面驗(yàn)證了胰島素增敏劑的作用,還發(fā)現(xiàn)了GATA4、HOXD3等潛在新藥靶點(diǎn),并提示甜菜堿、替米沙坦及抗炎藥阿塔西普等或具治療潛力。
綜上,該研究首次在中國(guó)與歐洲多祖先群體中系統(tǒng)揭示了PCOS的遺傳結(jié)構(gòu),發(fā)現(xiàn)了大量新風(fēng)險(xiǎn)位點(diǎn),并從遺傳角度揭示了PCOS的病理機(jī)制與藥物靶點(diǎn)。這些發(fā)現(xiàn)不僅深化了對(duì)PCOS遺傳基礎(chǔ)的理解,也為后續(xù)功能實(shí)驗(yàn)、臨床轉(zhuǎn)化及個(gè)體化治療提供了重要依據(jù)。未來(lái),結(jié)合更多人群數(shù)據(jù)、開(kāi)展細(xì)胞與動(dòng)物模型驗(yàn)證、推動(dòng)遺傳指導(dǎo)的臨床試驗(yàn),有望實(shí)現(xiàn)PCOS的精準(zhǔn)預(yù)防與治療。
中國(guó)科學(xué)院腦智卓越中心/上海交通大學(xué)Bio-X研究院師詠勇研究員、生殖醫(yī)學(xué)與子代健康全國(guó)重點(diǎn)實(shí)驗(yàn)室趙涵教授、青島大學(xué)/青島大學(xué)附屬醫(yī)院李志強(qiáng)教授、安徽醫(yī)科大學(xué)曹云霞教授為論文共同通訊作者。賀林院士、陳子江院士、黑龍江中醫(yī)藥大學(xué)吳效科主任對(duì)該研究給予了重要支持。生殖醫(yī)學(xué)與子代健康全國(guó)重點(diǎn)實(shí)驗(yàn)室趙涵教授和趙世剛教授、上海交通大學(xué)Bio-X研究院張曼菲副教授、安徽醫(yī)科大學(xué)徐玉萍主任、青島大學(xué)公共衛(wèi)生學(xué)院碩士研究生薛佰強(qiáng)為論文共同第一作者。
 附件下載:
附件下載: